- 《答聶文蔚》 [2017/04]
- 奧巴馬致女友:我每天都和男人做愛 [2023/11]
- 愛國者的喜訊,干吃福利的綠卡族回國希望大增 [2017/01]
- 周五落軌的真的是個華女 [2017/03]
- 現場! 全副武裝的警察突入燕郊 [2017/12]
- 法拉盛的「雞街」剛剛又鬧出人命 [2017/11]
- 大部分人品太差了--- 中國公園裡的「黃昏戀」 [2019/12]
- 亞裔男孩再讓美國瘋狂 [2018/09]
- 年三十工作/小媳婦好嗎 /土撥鼠真屌/美華素質高? [2019/02]
- 看這些入籍美加的中國人在這裡的醜態百出下場可期 [2019/11]
- 黑暗時代的明燈 [2017/01]
- 文革宣傳畫名作選之 「群醜圖」 都畫了誰? [2024/01]
- 當今的美國是不是還從根本上支持中國的民主運動? [2017/10]
- 香港的抗爭再次告訴世人 [2019/06]
- 中國女歡呼日本地震 歐洲老公驚呆上網反思 [2024/01]
- 加入外國籍,你還是不是中國人?談多數華人的愚昧和少數華人的覺醒 [2018/02]
- 周末逛法拉盛,還是坐地鐵? [2017/10]
- 春蠶到死絲方斷, 丹心未酬血已干 [2017/03]
研究人員發現一種遺傳傾向會增加乳腺癌轉移的風險
2024 年 12 月 9 日facebook 分享按鈕twitter 分享按鈕linkedin 分享按鈕電子郵件分享按鈕分享
複製鏈接圖標複製鏈接
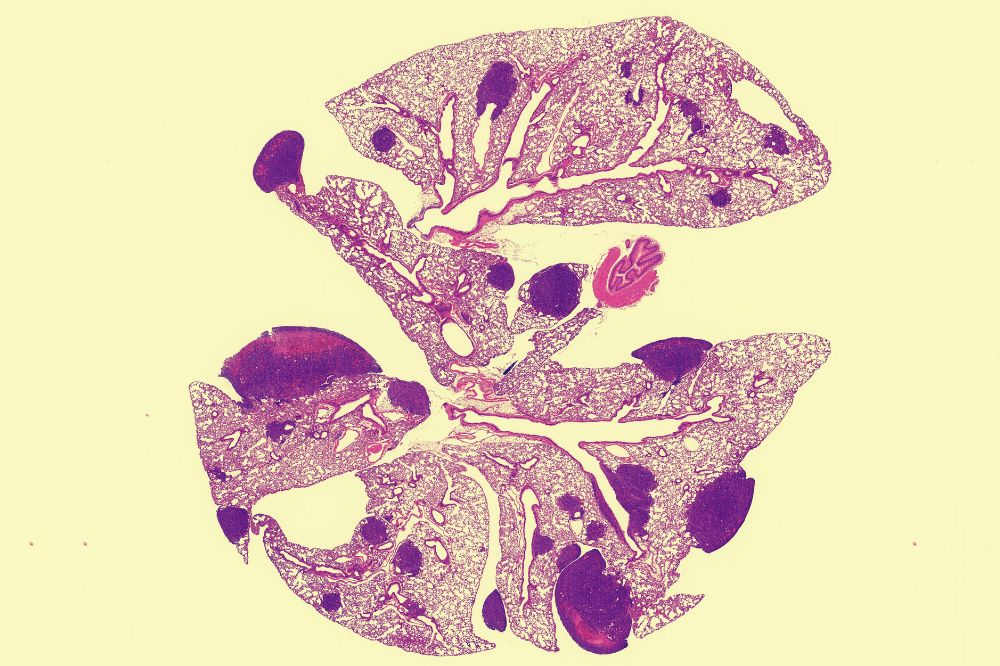
Tavazoie 實驗室組織學圖像當小鼠被設計成攜帶人類 PCSK9 基因的變體時,它們的乳腺癌轉移率會更高,從這張顯示 PCSK9 影響的小鼠肺組織圖像中可以看出。(Tavazoie 實驗室)
90% 的癌症死亡是由於癌症擴散,而不是原發腫瘤的併發症。因此,50 多年來,科學家們一直在探索腫瘤內哪些惡性突變可以讓流氓細胞脫離原發腫瘤,並通過血液和淋巴系統轉移到全身。
但新的研究表明,另一種機制被忽視了——驅動轉移的難以捉摸的突變可能不是在腫瘤本身的扭曲 DNA 中發展,而是在患者的正常遺傳 DNA 中發展。這項發表在《細胞》雜誌上的研究結果首次提供了乳腺癌轉移的遺傳易感性證據,具有深遠的臨床意義——包括一種可能預防轉移的治療方法。
「我們認為轉移至少在一定程度上是一種遺傳性疾病,」洛克菲勒大學的 Leon Hess 教授 Sohail Tavazoie 說。「我們過於關注癌細胞,即『種子』,而忽略了生殖細胞——『土壤』。現在很明顯,關注土壤至關重要。」
問題的根源
儘管科學家們幾十年來一直在嚴格研究轉移,但對轉移性腫瘤的廣泛基因組測序卻一無所獲。患者腫瘤中充滿了突變基因,但沒有一個被證明能特異性地驅動轉移。 「因此,我們假設,可能是宿主自身的基因,而不是腫瘤,導致了這些突變,」Tavazoie 說。
事實上,Tavazoie 及其同事此前已證明,APOE 的各種種系等位基因可以增強或抑制黑色素瘤轉移。為了查明乳腺癌轉移是否以類似的方式運作,Tavazoie 實驗室對來自多個國家的大量患者進行了人類遺傳學研究。
PCSK9 基因的一種常見變體立即引起了他們的注意。這種基因變體存在於 70% 的白人女性的種系中,與乳腺癌存活率降低有關。當該團隊用人類 PCSK9 的相關變體改造小鼠時,轉移率增加了。瑞典隆德大學的同事通過對大量斯堪的納維亞早期乳腺癌患者的分析進一步驗證了這些結果。他們的發現十分驚人:攜帶 PCSK9 變異的患者在 15 年內面臨 22% 的轉移風險,而未攜帶 PCSK9 變異的患者風險僅為 2%。
「我們的研究結果強調了國際合作的重要性,從定義上講,國際合作涉及來自多個國家的研究人員和患者群體,」Tavazoie 實驗室的研究生、論文第一作者 Wenbin Mei 說道。「此外,這還表明人類遺傳學已經變得多麼強大。隨著新技術將計算分析與實驗模型相結合,我們正處於一個解答難題的偉大時代。」
深入挖掘
該研究由 Hess 家族基金會和美國國家癌症研究所資助,還揭示了 PCSK9 變異如何驅動轉移。通過降解癌細胞上的 LRP1 受體,該變異似乎會引發一系列基因激活,這對於轉移啟動非常理想。有趣的是,該實驗室之前對黑色素瘤的研究發現,促進或抑制轉移的 APOE 等位基因也作用於 LRP1。「值得注意的是,在兩種不同的癌症中,轉移機制都集中在這個受體上,」Tavazoie 說。實驗室未來的工作將集中在 LRP1 在轉移中可疑的一致作用上。
儘管現在有證據表明 PCSK9 變異與轉移性疾病有關,但 Tavazoie 澄清說,患有這種變異的患者不應驚慌。數據顯示,患有這種變異的患者轉移風險為 22%,而沒有這種變異的患者轉移風險為 2%。「大多數患有早期乳腺癌且攜帶這兩種變異的患者都不會發生轉移,」他說。
但他現在對減少攜帶這種變異患者的轉移性疾病的可能性持樂觀態度。本研究包括初步工作,表明可以使用一種阻斷 PCSK9 活性的抗體來抑制 PCSK9,這種抗體已經獲批用於治療高膽固醇。 「這是一種安全且耐受性良好的藥物,」塔瓦佐伊說,同時提醒說,需要進行臨床試驗來證明其對癌症的療效。「我們希望有朝一日,攜帶這種變異的高危患者能夠得到積極治療,從而降低他們患癌症的幾率。」
- [03/22]AOC、沃爾茲、吳——這些瘋子是民主黨的未來?!
- [03/22]退休年齡推遲到60歲,青年就業減少16%」
- [03/22]Maher to meet Trump @White House//Kotlik named Cornell』s 15th prez
- [03/23]川普向深層搞鬼訟棍大律師團伙宣戰先下一城 這些貨的反應是?
- [03/23]肯尼迪藝術中心項目總監全裸上網怒批川普瞎搞
- [03/23] 研究人員發現一種遺傳傾向會增加乳腺癌轉移的風險
- [03/24]川普新政—恢復傳統 重塑現狀
- [03/24]欣賞劉貫道的《消夏圖》
- [03/24]新發現-為什麼你的耳機電池續航時間不長
- [03/25]關閉教育部!川普又發瘋了?
- [03/25]風流之情 悠悠 田家之心 涼涼
- [03/26]世紀快閃 來得準時 走得隨機 芳名有千數 塵世無萬日
- [03/26]【再回首】在戰火中搶救了居延漢簡的徐森玉先生
- 查看:[change?的.最新博文]
- 查看:[大家的.最新博文]
- 查看:[大家的.健康生活]
評論 (0 個評論)
change?最受歡迎的博文
其它[健康生活]博文更多
- 玉米穗:關於喝茶
- change?:日本美國二月報道胰腺癌早期檢測可突破
- 8288:老了就是老了,好好活著,
- change?:從不休息不過年每天半夜后休息的99歲小鎮醫生-謝春梅
- 老地雷:我得了個冠軍、贏了個大獎
- 8288:一次生氣,居然能氣出20多種病
- 8288:《窮極一生,追求的是什麼?》
- qwxqwsean:今天來重症室看望母親又發現醫生瞎搞
- qwxqwsean:昨天去重症室看望母親
- qwxqwsean:母親就這麼突然完蛋了
- qwxqwsean:我不明白為啥除我之外的其他人都是傻查
- qwxqwsean:昨天去法拉盛看望母親
- qwxqwsean:今天去看望母親
- 玉米穗:關於喝酒
- qwxqwsean:醫院拒絕為母親治療,踢出去不管了
- change?:紐約 70 歲老人分享對年輕自我的建議
- bobzhou:中醫針灸和中醫藥在美國的狀況是這樣嗎
- cuihanjuk:記憶力減退的原因及解決方法
- change?:來了!俄州成美首報小兒肺炎病例神增州
- 8288:在美國如何修正醫療賬單收費錯誤








